
உலகம் முழுதும் பொதுவாக ஒரு மாத்திரை அல்லது மருந்தை, ஒரு நாட்டில் சந்தைபடுத்தும் போது, சர்வதேச விதிப்படி, அந்த மருந்து clinical trial எனப்படும் மருத்துவ சோதனை (கட்டம் )1, 2, 3 ஆகிவற்றை கட்டாயம் வெற்றிகரமாக கடந்து வந்தபின் தான் நோயாளிகள் உபயோகத்திற்குச் சந்தை படுத்த முடியும். இந்த சோதனை நடத்த பெரிய அளவில், கோடிக்கணக்கில் செலவு செய்யவேண்டும். இதுதான் சர்வதேச அளவில் மருந்து சந்தைபடுத்தும் நடைமுறை. இந்த தகவலுடன் தொடருவோம்…….

படம்: patinetslikeme
என் தாய்த் திருநாடுதான் உலகத்தின் குப்பைக்கிடங்கு, சோதனைக் கூடம்.
உலக நாடுகள் இந்தியாவை ஒரு சோதனைக் களமாக மாற்றிக் கொண்டிருக்கிறது. எங்கெல்லாம் தயாரிக்கப்படும் மாத்திரை மருந்துகள் தடை செய்யப்படுகிறதோ , அதை இந்தியாவில் இருக்கும் சில திருட்டு அரசியல்வாதிகள் மூலமும் பணத்திற்கு நாக்கை நீட்டும் (நாக்கை மட்டுமா) மருத்துவ சமுதாயத்தில் உள்ள கருப்பு ஆடுகளைப் பிடித்து , இங்கே அந்த மருந்துகளை எல்லாம் விற்று விடுகிறார்கள். இதில் முக்கியப் பங்கு விபச்சாரம் செய்யும் விளம்பரதாரர்களும், தன் சுயநலன் மட்டும் பேணும், விபரம் இல்லாத முட்டாள் மக்களும் வாங்கிப் பயன்படுத்தி அதை ஒரு நல்ல மருந்து என்ற கோணத்திற்கு கொண்டு சென்று விடுகிறார்கள்.
உலக மருத்துவ ஆராய்ச்சி கழகத்தால் உபயோகப்படுத்தக் கூடாது என்று ஒழித்துக் கட்டப்பட்ட பல மாத்திரைகளைத்தான் இன்று நாம் உட்கொள்கிறோம்
ஒரு சிறு உதாரணம்: இன்று தலைவலி , ஜலதோஷம் என்றவுடன் மக்கள் (அந்த முட்டாள் மக்களிள் நானும் ஒருவன்தான் ) முதலில் வாங்குவது Vicks Action 500 மாத்திரைதான். இதன் பாதிப்பு பற்றித் தெரியுமா? இது மாரடைப்பை உடனே தூண்டும் சக்தி கொண்ட து

படம்: indiatimes
இந்தியாவில் பல மிகவும் பிரபலமான மருந்துகள், அதன் பாதுகாப்பு அம்சம் பற்றிச் சரியான மருத்துவ சோதனைகள் செய்யப்படாமல், விற்கப்படுகின்றன. அவ்வாறு விற்று மக்களை அந்த மருந்துகளை, உட்கொணர வைப்பது, அவர்களை ஆய்வக மிருகமாக நடத்துவதற்கு சமம். இதை நாமாகச் சொல்லவில்லை, நாட்டின் மருந்துக்கான மிகப்பெரிய கட்டுபாட்டு அமைப்பான Central Drugs Standard Control Organisation (CDSCO )-வின் செயல்பாடுகளை ஆய்வு செய்த, சுகாதாரம் மற்றும் மக்கள் நல்வாழ்வுக்கான நாடாளுமன்ற நிலைக்குழு தனது அறிக்கையில் இவ்வாறு தெரிவித்து உள்ளது.
33 புதிய மருந்துகளுக்கு ஜனவரி 2008 முதல் அக்டோபர் 2010 வரை, எந்தவித மனித சோதனை ஆய்வுமின்றி ஒப்புதல் அளிக்கப்பட்டுள்ளன. இந்த நிலைக்குழு அறிக்கைப்படி, சராசரியாக மாதம் ஒரு மருந்திற்கு எந்தவித மனித சோதனையுமின்றி Drug Controller General of India (DCGI) அனுமதி அளித்துள்ளது.
தனியாக 39 மருந்துகள் தோராயமாகத் தேர்வு செய்யப்பட்டுப் பார்த்ததில், 11 மருந்துகள் (28 %) அத்தியாவசியமான கட்டம் 3rd clinical trial என்னும் மூன்றாம் கட்ட மருத்துவ சோதனை செய்யப்படவில்லை. இதில் சில மருந்துகள், மிகப் புகழ்பெற்ற மருந்து நிறுவனங்களான நோவர்டிஸ், சிப்லா, எளிலில்லி-யின் மருந்துகள். பொதுவாக இந்த சோதனைகள், குறைந்தது 100 நோயாளிகளிடம் சோதனை செய்யப்பட வேண்டும். ஆனால் பன்னாட்டு மருந்து நிறுவனமான சனோபி நிறுவனத்தின் Dronedarone என்ற மருந்து வெறும் 21 பேரிடமும், நோவார்டிஸ் நிறுவனத்தின் அலிஷ்கிரன் மருந்து வெறும் 46 பேரிடம் மட்டும் தான் பாதுகாப்பு பற்றிச் சோதனை செய்யப்பட்டுள்ளது. இது அப்பட்டமான விதி மீறல் பொதுவாக இதுபோன்ற சோதனை 3 அல்லது 4 மருத்துவமனைகளில் சோதனை செய்யவேண்டும் என்பது விதி. ஆனால் Macleod நிறுவனத்தின் Irsogladine மருந்து, வெறும் 2 மருத்துவமனைகளில் மட்டும் தான் சோதனை செய்யப்பட்டதாக தெரிகிறது.
இன்னும் மிகப் பிரபல நிறுவனகளின் 4 மருந்துகள் (Everolimus of Novartis, Buclizine of UCB, Pemetexid of Eli Lilly and FDC of Pregabalin) மூன்றாம் கட்ட மருத்துவ சோதனை செய்யப்படவில்லை. அதுபோக, கட்டாயம் பெறவேண்டிய expert opinion என்னும் வல்லுநர் கருத்து பெறப்படவும் இல்லை. இதுவும் அப்பட்டமான விதிமீறல். CDSCO அமைப்பின் மருத்துவம் சாராத அலுவலர்கள் இந்த ஒப்புதலை தனிச்சையாக அளித்ததாக தெரிகிறது.
இதனால் இந்திய நோயாளிகளின் பாதுகாப்பு அம்சம் கேள்விக்குறி ஆக்கப்பட்டுள்ளது.
இன்னும் அந்த அறிக்கைப்படி, 13 (33%) மருந்துகளுக்கு மிக வளர்ந்த நாடுகளான அமெரிக்கா, கனடா, ஐரோபிய நாடுகள், ஆஸ்திரேலியா போன்றவை அனுமதி அளிக்கவில்லை. இந்த மருந்துகளுக்கு இந்தியாவில் மருத்துவ தேவை இல்லவே இல்லை. 25 மருந்துகளுக்கு (64 %) ஒப்புதல் பெறுமுன் அவசியம் பெறவேண்டிய மருத்துவ வல்லுநர் கருத்து முழு அளவில் பெறப்படவில்லை. மிகச் சாதாரணமாக காய்ச்சலுக்குப் பயன்படுதப்படும், PARACETAMOL என்னும் காய்ச்சலை குறைக்கும் மருந்துகளின் DOSE மறுமதிப்பீடு செய்ய மட்டும், USFDA என்னும் அமெரிக்காவின் மருந்து கட்டுப்பாட்டுக் கழகம் 37 நபர் கொண்ட மருத்துவ வல்லுனர்களை அமைத்தது என்றால் இதன் முக்கியத்துவம் புரிகிறதா?.
“பொது நலன் கருதிச் சட்டப்படி DCGI க்கு சில மருந்துகளுக்கு மருத்துவ சோதனை இல்லாமல் அனுமதி கொடுக்க அனுமதி உண்டு ” என்று இந்திய மத்திய சுகாதார அமைச்சகம் கூறுகிறது. ஆனால் பொது நலன் என்பதற்கு எந்த விரிவான விளக்கமும் இல்லை. இந்த சட்டத்தின் ஓட்டையைத்தான் பல மருந்து நிறுவனங்கள் தவறாகப் பயன்படுத்திக்கொண்டு பாதுகாப்பு சோதனை, வல்லுநர் கருத்து, போன்றவற்றைப் பெறாமல் சந்தைப் படுத்துகிறது. அப்போது ‘பொது நலம்’ என்றால் என்ன என்று நாம் விளங்கிக்கொள்ள வேண்டியதுதான்.

படம்:pharmacovigilance
வெளிநாட்டு மருந்துகளுக்கு இந்தியாவில் மருத்துவ சோதனை செய்யாமல் கொடுத்தது எப்படி பொது நலம் ஆகும். அந்த மருந்துகளை வெளிநாடுகளில் உள்ள நோயாளிகளிடம் தகுந்த சோதனைக்கு பின்னரே சந்தைப்படுத்துகின்றனர். ஆனால் அங்கு நடத்திய சோதனை நம் நாட்டுச் சூழலில் ஒத்து வருமா? என்று சொல்ல முடியாது. அதனால்தான் இங்கும் அதுபோல் மருத்துவ பாதுகாப்பு சோதனைகள் செய்யப்படவேண்டும்.
Daptomycin (Cubicin) of Novartis 2003 செப்டம்பர் மாதம் வெளிநாட்டில் சந்தைப் படுத்தப்பட்டது. இந்தியாவில் நான்கு ஆண்டுக்குப் பிறகு Jan 28, 2008 தான் ஒப்புதல் வழங்கப்பட்டது. இந்த நான்கு வருடங்களில் இந்தியாவில் மருத்துவ சோதனை செய்திருக்கலாம். ஆனால் ஏன் இந்த அலட்சியம்?
Pemetrexed (Alimta) of Eli Lilly என்ற மருந்திற்கு அமெரிக்காவில் பிப்ரவரி 5-2004 இல் ஒப்புதல் அளிக்கப்பட்டது. இந்தியாவில் இரண்டு வருடம் கழித்து ஜூன் 28, 2006 இல் அதே மருந்திற்கு எவ்வித சோதனையும் இன்றி DCGI யால் ஒப்புதல் அளிக்கபட்டது. போதுமான நேரம் இருந்தும் சோதனை செய்யப்படாமல், அந்த மருந்துக்கான அவசர அத்தியாவசியமும் இல்லாமல், தயாரிக்கும் நிறுவனத்தின் இலாபத்திற்காக ஒப்புதல் அளிக்கப்பட்டுள்ளது.
DRUGS WHOSE MANDATORY PHASE III TRIALS WERE NOT HELD Everolimus (Novartis) Colistimethate (Cipla) Exemestane (Pharmacia) Buclizine (UCB) Pemetrexid (Eli Lilly) Aliskiren (Novartis) Pentosan (West Coast) Ambrisentan (GlaxoSmithKline) Ademetionine (Akums) Pirfenidone (Cipla) FDC of Pregabalin, Methylcobolamine, Alpha Lipoic Acid, Pyridoxine & FolicAcid (Theon)
இந்தப் பட்டியல் நிலைக்குழு ஆராய்ந்தது மட்டும்தான். இன்னும் எத்தனை மருந்துகள் இப்படி இந்தியாவில் சந்தை படுத்தப்பட்டதோ ?
குழந்தையின்மைக்காக பயன்படுத்தப்படும் LETROZOLE என்னும் மருந்திற்கு Central Drugs Standard Control Organization (CDSCO) அமைப்பால் சட்ட விதிகளை மீறி ஒப்புதல் அளிக்கப்பட்டுள்ளது. இதற்காகப் பாராளுமன்ற நிலைக்குழு இதில் ஈடுபட்டவர்கள் மீது நடவடிக்கை எடுக்கப் பரிந்துரைத்துள்ளது. சர்வதேச அளவில் இந்த மருந்திற்கு மார்பக புற்றுநோய்க்காக மட்டுமே பயன்படுத்த ஒப்புதல் உள்ளது. ஆனால் இந்தியாவில் குழந்தை இல்லாத சிறுவயதுப் பெண்களுக்கு பயன்படுத்த ஒப்புதல் அளிக்கப்பட்டுப் பயன்படுத்தப்பட்டு வருகிறது. இந்த மருந்தைப் பயன்படுத்திக் கருவுறும் குழந்தைகளுக்குப் பிறவிக் குறைபாடு என்னும் பக்க விளைவு வரும் வாய்ப்பு உள்ளது. அண்மையில்தான் இந்த மருந்தைக் குழந்தையின்மைக்குப் பயன்படுத்த இந்திய அரசு தடை செய்துள்ளது.
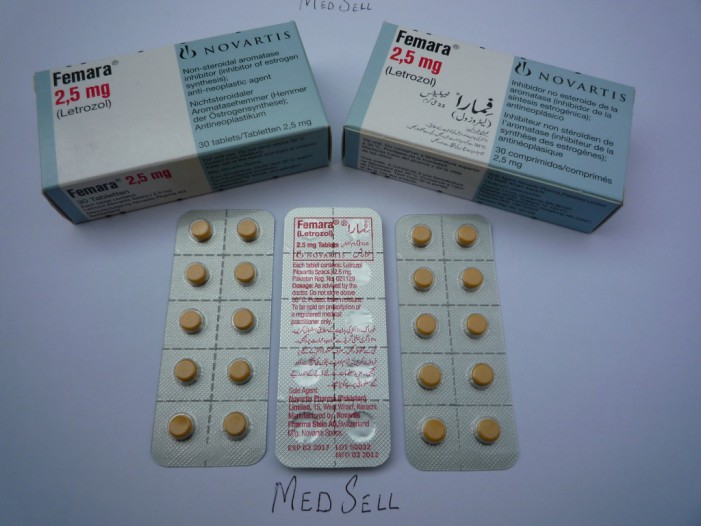
படம்: medsell
இந்த மருந்தை மாதவிடாய் நின்ற பெண்கள் மட்டுமே உபயோகப்படுத்த வேண்டும். இனப்பெருக்கத் தகுதி வயதில் உபயோகப்படுத்தவே கூடாது என்றுள்ளது. ஆனால் ஏப்ரல் 10, 2007 அன்று ‘The Drug Controller General’of India’ பெண்களின் மலட்டுத் தன்மைக்காகப் பயன்படுத்த இந்த மருந்திற்கு எப்படி அனுமதி அளித்தது என்று தெரியவில்லை.
அமெரிக்காவில் USFDA மருந்து கட்டுப்பாட்டுத் துறையில் phenylpropanolamine என்ற மருந்தின் பாதிப்பை எவ்வாறு கையாண்டது என்று பார்ப்போம். இந்த மூலக்கூறு சாதாரணமாக தும்மல், காய்ச்சல் , இருமல் மருந்துகளில் ஒரு பகுதியாக கிட்டத்தட்ட 20 ஆண்டு காலமாக இந்தியா போன்ற நாடுகளில் பயன்படுத்தப்படுகிறது. இதன் குணாதிசியம் என்னவென்றால்இ து மூக்கில் அடைப்புத் தன்மையை போக்க வல்லது (nasal decongestant ), மேலும் உடல் எடையைக் குறைக்கவும், பசியை குறைக்கவும் குறைந்த அளவில் பயன்படுத்தப்பட்டு வந்தது. மே 11, 2000 அன்று அமெரிக்காவின் மருந்துக் கட்டுப்பாட்டுத் துறையான USFDA அமைப்புக்கு YALE University School of Medicine என்ற பல்கலைக்கழக விஞ்ஞானிகள் ஆய்வு அறிக்கை ஒன்று அனுப்பியது. அந்த அறிக்கை மிகவும் அதிர்ச்சியூட்டுவதாக இருந்தது. அந்த ஆராய்ச்சியில் phenylpropanolamine உபயோகப்படுத்திய பல பெண்களுக்கு மூளையில் இரத்தக் கசிவு ஏற்பட்டு STROKE என்னும் வாத நோயை உண்டு பண்ணியதாகக் கூறியது. அதோடு HAEMORRHAGIC STROKE என்னும் இரத்த கசிவு நோய் ஆண்களுக்கும் வரும் வாய்ப்பு உண்டு என்று தெரிவித்திருந்தது. உடனே நவம்பர் 6 ,2000 ஆண்டு USFDA இந்த மருந்தை மூலக்கூறாகப் பயன்படுத்தும் அனைத்து நிறுவனங்களையும் இந்த மருந்தைத் தானாகவே மருந்துச் சந்தையில் இருந்து விலக்கிக் கொள்ளும்படி அறிவுறித்தி, பின்னர் அதைச் சட்டமாகியது.
- மிக முக்கிய குறிப்பு ஜி7( கனடா, ப்ரான்ஷ்,ஜெர்மனி,இத்தாலி, ஜப்பான், லண்டன், அமெரிக்கா, யுரோப்பியன் யூனியன்) நாடுகளில் ஒரு மருத்துவர் நோயாளிகளுக்கான மருந்தை எழுதி தர முடியாது என்ன நோய் என்று கண்டறிந்து அதை மட்டுமே எழுதித்தர முடியும், பின் மருந்துக்கான மருத்துவ நிபுணர்கள் தான் மருந்தை தர முடியும்
- இப்படி இருக்க மனித உயிருடன் விளையாடி, போதுமான மருத்துவ சோதனை இல்லாத மருந்துகளுக்கு அனுமதி கொடுத்தவர்களைச் சட்டத்தின் முன் நிறுத்தி நமது அரசு தண்டனை பெற்றுத் தர வேண்டும்.
உசாத்துணைகள்:
- Drugs,DrugSafety and Information by Drug Class.
- டாக்டர் த முஹம்மது கிஸார் அவர்கள் காணொளி மற்றும் கட்டுரைகள்.







