
শিশুকাল থেকেই দুটো বিষয়ে নীলস বোর সকলের চেয়ে এগিয়ে ছিলেন। একটি গণিত, অপরটি মারামারি! গণিতে অসামান্য দক্ষতার জন্যই হয়তোবা ধীরে ধীরে তিনি পদার্থবিজ্ঞানের প্রতি আসক্ত হয়ে ওঠেন। আর পদার্থবিজ্ঞানেও তিনি দ্রুতই ‘মাস্টার’ হয়ে ওঠেন। কেমন মাস্টার? মাধ্যমিক স্কুলে পড়াকালীনই তিনি মাধ্যমিক পদার্থবিজ্ঞান বইয়ের ভুল শুধরে দিয়েছিলেন, একটি দুটি নয়, অনেকগুলো! আর গণিতের প্রতিভার মতোই তার স্বাস্থ্যও ছিল অস্বাভাবিকভাবে ভালো। গায়ে যেন ছিল অসুরের শক্তি! বইয়ের ভুল ঠিক করবার পাশাপাশি তিনি স্কুলের বখাটে ছেলেপেলেদেরও মেরে মেরে ‘ঠিক’ করতেন!

কিশোর নীলস বোর; source: corespirit.com
১৯০৫ সালের ফেব্রুয়ারি মাস। নীলস বোর তখন ২০ বছর বয়সী এক টগবগে যুবক। পদার্থবিজ্ঞানের প্রতি এই যুবকের আকর্ষণ তখন, জুলিয়েটের প্রতি রোমিওর আকর্ষণকেও হার মানাতো। এমন সময় ‘দ্য রয়্যাল ড্যানিশ একাডেমি অব সায়েন্স’ থেকে, তরলের পৃষ্ঠচাপ নির্ণয়ের পদ্ধতি সম্পর্কিত সেরা গবেষণাপত্রের জন্য স্বর্ণপদক ঘোষণা করা হলো। এই প্রতিযোগিতাটি ছিল কেবল অভিজ্ঞ বিজ্ঞানী এবং উচ্চতর (পি.এইচডি) ডিগ্রির জন্য গবেষণারতদের জন্য। সেখানে স্নাতক পড়ুয়া বোর সিদ্ধান্ত নিলেন এই প্রতিযোগিতায় তিনি অংশগ্রহণ করবেন! নিজের প্রফেসর বাবার দ্বারা তিনি প্রতিযোগিতায় অংশগ্রহণের ব্যবস্থা করালেন।
ছেলের উদ্দীপনা দেখে চমৎকৃত হন বাবা ক্রিশ্চিয়ান বোর। তিনি নিজের বিশ্ববিদ্যালয়ের গবেষণাগারটি বোরের জন্য উন্মুক্ত করে দেন। বোর সেখানে পাগলের মতো দিন-রাত কাজ করতে শুরু করেন। কয়েকদিনের মধ্যেই ছেলের এই হাড়ভাঙা পরিশ্রমে চিন্তিত হয়ে পড়েন ক্রিশ্চিয়ান বোর। তিনি ছেলের প্রচেষ্টা এবং আগ্রহের প্রশংসা করেন, তবে গবেষণা থামিয়ে দিতে বলেন। কিন্তু বোর কি এ কথা শোনার পাত্র? তিনি তার গবেষণার অবশিষ্ট কাজটা সেরে ফেলতে চলে যান নানাবাড়ি। আর তার ধনাঢ্য নানা, নাতির গবেষণার জন্য ব্যবস্থা করে দিতে কোনো কার্পণ্য করলেন না। ১৯০৬ সালের অক্টোবর মাসে বোর তার গবেষণাপত্র জমা দেন। এবং তিনিই সব অভিজ্ঞদের হারিয়ে স্বর্ণপদক জিতে নেন!

কোপেনহেগেন বিশ্ববিদ্যালয়; source: .bu.edu
ড্যানিশ একাডেমির স্বর্ণপদক জিতে নিজের আগমনী বার্তা বিজ্ঞান বিশ্বকে দিয়ে ফেলেছিলেন বোর। স্নাতক শেষ করার পর, এই প্রতিভাধর যুবক তাই পেয়ে যান ইংল্যান্ডের ক্যামব্রিজ বিশ্ববিদ্যালয়ে গবেষণার সুযোগ। ১৯১১ সালের অক্টোবরে তিনি ইংল্যান্ড পৌঁছেন। সৌভাগ্যক্রমে, জে. জে থমসনের সাথে ক্যাভেন্ডিস ল্যাবরেটরিতে কাজ করার সুযোগ পান বোর। কিন্তু সবকিছুই যেন গোল পাকিয়ে গেল। বোরের পছন্দ হলো না গবেষণার গুরু থমসনকে, আর থমসনের পছন্দ হলো না শিষ্যকে! ফলাফল? ক্যাভেন্ডিস ল্যাবরেটরি ত্যাগ করার সিদ্ধান্ত নেন বোর।
ম্যানচেস্টার বিশ্ববিদ্যালয়ে আর্নেস্ট রাদারফোর্ডের সাথে, তার গবেষণাগারে কাজ করবার অনুমতি চাইলেন বোর। রাদারফোর্ড রাজি হয়ে গেলেন। আর থমসন তো বিদায় করতে পারলেই বাঁচেন, তাই দিয়ে দিলেন অনুমতি! ১৯১২ সালে নতুন আশা নিয়ে ম্যানচেস্টারে পাড়ি জমালেন বোর। ১৯০৮ সালের রসায়নে নোবেল পুরস্কার জিতেছিলেন রাদারফোর্ড। এমন একজন খ্যাতিমান বিজ্ঞানীর সাথে কাজ করার সুযোগ পেয়ে বোর ছিলেন উচ্ছ্বসিত।

আরনল্ড সমারফিল্ডের সাথে নীলস বোর; source: bu.edu
রাদারফোর্ডের সাথে প্রায় এক বছর কাজ করেন বোর। গবেষণা সম্পন্ন করে যখন তিনি দেশে ফেরেন, তখন রাদারফোর্ডের একটি গুণ তার মধ্যেও সংক্রমিত হয়ে গেছে। আর তা হচ্ছে সমালোচনায় কান না দেয়া। শত সমালোচনার মাঝেও নিজের ‘ধনাত্মক চার্জিত নিউক্লিয়াস’ তত্ত্বের সাথে লেগে থাকেন রাদারফোর্ড। আর এই ব্যাপারটিই অনুপ্রাণিত করে বোরকে। ১৯১২ সালে তিনি ডেনমার্ক ফেরেন। তখন তার একটাই লক্ষ্য ছিল, আর তা হচ্ছে পরমাণুতে ইলেকট্রনের ধর্ম বোঝার চেষ্টা করা।
দেশে ফিরেই বোর কোপেনহেগেন বিশ্ববিদ্যালয়ে অধ্যাপক হিসেবে যোগ দেন। পাশাপাশি পরমাণুতে ইলেকট্রনের অবস্থান নিয়ে গবেষণা চালিয়ে যান। রাদারফোর্ডের ধনাত্মক নিউক্লিয়াস তত্ত্ব, ক্লাসিক্যাল পদার্থবিজ্ঞান দ্বারা কোনোভাবেই সমর্থিত হয়নি। কারণ, নিউক্লিয়াস ধনাত্মক হলে ঋণাত্মক চার্জবিশিষ্ট ইলেকট্রন তো সব নিউক্লিয়াসে গিয়ে পড়ার কথা। কিন্তু ইলেকট্রন তো দিব্যি ঘুরে চলেছে নিউক্লিয়াসের বাইরে। বোর ইলেকট্রনের এই অস্বাভাবিক আচরণ নিয়ে ভাবতে শুরু করেন। তিনি ম্যাক্স প্ল্যাঙ্কের কোয়ান্টাম তত্ত্ব দিয়ে এই সমস্যা দূর করবার প্রয়াস চালান। কিন্তু কিছুতেই কিছু হচ্ছিল না। ইলেকট্রনের আচরণ ব্যাখ্যার সাথে কোয়ান্টাম তত্ত্বের সাযুজ্য প্রমাণে তিনি দিনরাত এক করে দেন। ফলাফল ছিল শূন্য। হতোদ্যম বোরের নজরে হঠাৎ চলে আসে বামার সিরিজের ব্যাপারটি।
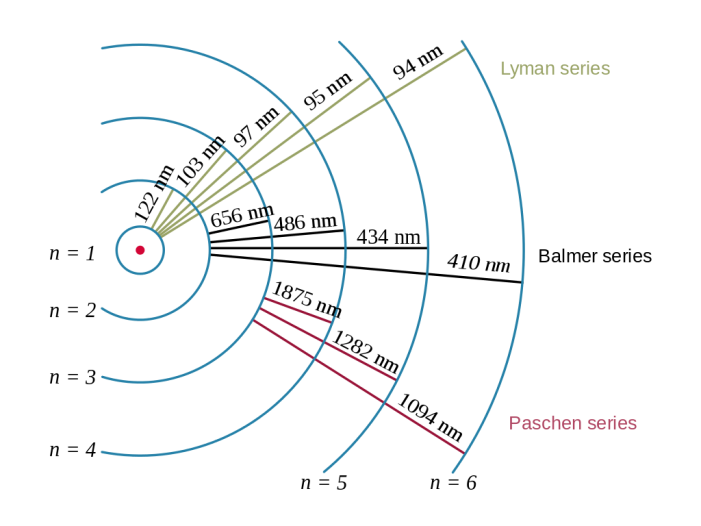
বামার সিরিজ; source: commons.wikimedia.org
১৮৮৫ সালে গণিতবিদ বামারের তৈরি সূত্রটির পেছনে কোনো তাত্ত্বিক ভিত্তি ছিল না। তথাপি সূত্রটি সঠিকভাবে তরঙ্গদৈর্ঘ্য নির্ণয় করতে সক্ষম হয়। এই ব্যাপারটিই বোরকে পুনরায় উৎসাহিত করলো। তিনি বামার সিরিজকেই প্রথমে কোয়ান্টাম তত্ত্ব দ্বারা প্রতিষ্ঠা করলেন। আর এতেই কাজের কাজ হয়ে গেল। বামারের সূত্রে তিনি প্ল্যাঙ্কের সূত্র ও ইলেকট্রনের ভর প্রতিস্থাপিত করলেন। এর ফলাফল হলো বিস্ময়কর। গাণিতিক ফলাফলকে সহজ ভাষায় বললে, একটি পরমাণু ঠিক সৌরজগতের মতো, যেখানে নিউক্লিয়াসকে ঘিরে ইলেকট্রনগুলো ‘নির্ধারিত’ কক্ষপথে আবর্তন করে। একই কক্ষপথে একাধিক ইলেকট্রন থাকতে পারে। তবে, যে ইলেকট্রন যত দূরের কক্ষপথে অবস্থান করবে, তার শক্তি তত বেশি হবে।
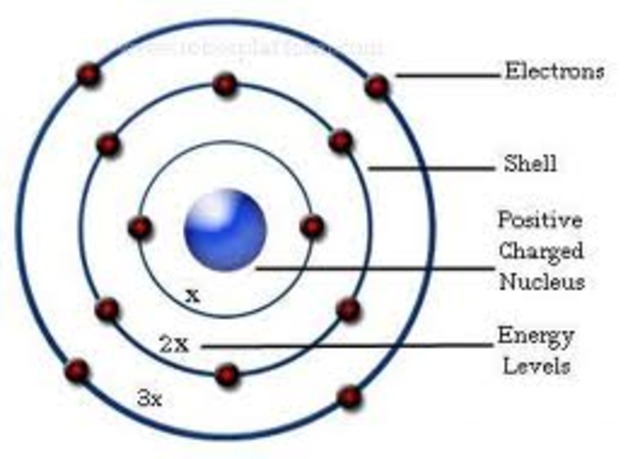
বোরের পরমাণু মডেল; source: timetoast.com
পদার্থ কীভাবে আলো শোষণ কিংবা নির্গত করতে পারে? দীর্ঘদিনের এই বৈজ্ঞানিক সমস্যাটির সমাধান ছিল বোরের নতুন মডেলে। বোরের মডেলে বলা হয়, নিম্নশক্তির কক্ষপথের ইলেকট্রনগুলো ফোটন বা শক্তি শোষণ করে, উচ্চশক্তির কক্ষপথে লাফিয়ে চলে যায়। আবার উচ্চ শক্তির কক্ষপথের ইলেকট্রনও শক্তি বা ফোটন নির্গত করে, নিচের কক্ষপথে নেমে যায়। যেখানে ক্লাসিক্যাল পদার্থবিজ্ঞানে ইলেকট্রন যেকোনো পরিমাণ শক্তি ধারণ করতে পারে বলে মনে করা হতো। সেখানে কোয়ান্টাম পদার্থবিজ্ঞানে এসে প্রতীয়মান হলো যে, ইলেকট্রনগুলো নির্দিষ্ট কক্ষপথে নির্দিষ্ট পরিমাণ শক্তি ধারণ করে থাকবে।
আর এই নির্দিষ্ট শক্তির জন্যই, একটি ইলেকট্রনের জন্য নিজের কক্ষপথ ছাড়া বাকিগুলো ‘ফরবিডেন জোন’ হয়ে যায়। কিন্তু ইলেকট্রন যখন ফোটন (শক্তির প্যাকেট বা কোয়ান্টা) শোষণ করে, তখন সেই ফরবিডেন জোনের সমপরিমাণ শক্তি সে পায় এবং সেখানে কোয়ান্টাম লাফ দিয়ে চলে যেতে সক্ষম হয়। এর দ্বারা ইলেকট্রনের ‘অস্বাভাবিক’ আচরণও স্বাভাবিক হয়ে যায়। ধনাত্মক নিউক্লিয়াসে গিয়ে না মিশে বরং এর চারদিকে ইলেকট্রন এজন্য আবর্তন করতে সক্ষম হয় যে, নিউক্লিয়াস ইলেকট্রনের জন্য একটি ফরবিডেন জোন এবং সেখানে যাবার মতো নির্দিষ্ট শক্তি ইলেকট্রন শোষণ কিংবা নির্গমন করতে পারে না।
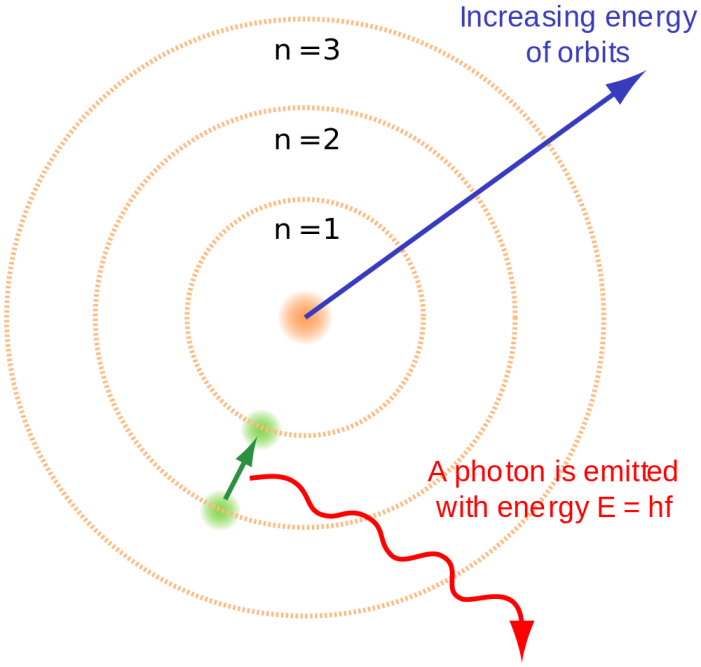
বোরের কোয়ান্টাম মডেল; source: commons.wikimedia.org
নীলস বোর এই তত্ত্বের মাধ্যমে একটি যুগান্তকারী আবিষ্কার করে ফেলেন। তিনি দেখান যে, পর্যায় সারণীতে অধিকাংশ মৌলের রাসায়নিক ধর্মগুলো মূলত এদের শেষ স্তরের ইলেকট্রন অর্থাৎ, যোজন (ভ্যালেন্স) ইলেকট্রন দ্বারা নির্ধারিত হচ্ছে। আর এই পর্যবেক্ষণের সাথেই তিনি বিজ্ঞানের এক নতুন দুয়ার উন্মোচন করেন, যার নাম ‘কোয়ান্টাম রসায়ন’। ১৯১২ সালে এই বিস্ময়কর আবিষ্কারের পর, ১৯১৩ সালে তিনি এতে সমীকরণ যুক্ত করেন। পরবর্তীতে, ১৯২০ সালে হাইজেনবার্গ ও স্রোডিংগার এর আরো উন্নয়ন সাধিত করেন।
১৯১৩ সালে নীলস বোর তার কোয়ান্টাম গবেষণাপত্র প্রকাশ করেন। সাথে সাথে নিজের তত্ত্বের মতোই তার সুনাম, কোয়ান্টাম লম্ফ দিয়ে অনেক উচ্চে প্রতিষ্ঠিত হয়। বিশ্বের নামিদামি সব বিশ্ববিদ্যালয় তাকে বক্তৃতা দিতে আমন্ত্রণ জানালো। তিনি সাগ্রহে সেগুলো গ্রহণ করতে লাগলেন। প্রথম বিশ্বযুদ্ধের সময় তিনি ম্যানচেস্টারে চলে যান। যুদ্ধ শেষে আবার কোপেনহেগেন বিশ্ববিদ্যালয়ে ফিরে আসেন এবং তাত্ত্বিক পদার্থবিজ্ঞানের চেয়ারম্যান হন। ১৯২২ সালে তাকে পদার্থবিজ্ঞানে নোবেল পুরস্কারে ভূষিত করা হয়।

নোবেল পুরস্কার গ্রহণের পূর্বে নীলস বোর; source: codepen.io
১৯৩২ সালে জেমস চ্যাডউইক নিউট্রন আবিষ্কার করেন। এর ফলে বোরের আকর্ষণ আরো একবার নিউক্লিয়াসের দিকে চলে যায়। তিনি একটি ‘কম্পাউন্ড নিউক্লিয়াস’ তত্ত্ব তৈরি করেন। এই তত্ত্ব অনুযায়ী, যখন কোনো নিউট্রন দ্বারা কোনো নিউক্লিয়াসকে আঘাত করা হয়, তখন সে নিউট্রনটি নিউক্লিয়াসের কেবল একটি নিউট্রনের সাথে সংঘর্ষে লিপ্ত হয় না। বরং তা ক্রমাগত নিউক্লিয়াসে অবস্থিত নিউট্রন ও প্রোটনের সাথে সংঘর্ষে লিপ্ত হতে থাকে এবং গামা রশ্মি কিংবা নিউট্রন আকারে শক্তি নির্গমন করে। শেষতক তা একটি ‘সেমি কম্পাউন্ড নিউক্লিয়াস’ তৈরি করে।
দ্বিতীয় বিশ্বযুদ্ধ চলাকালে, ১৯৪০ সালে জার্মানি ডেনমার্ক দখল করে। বোরের মা ইহুদী হওয়ায় সমস্যা হবার সম্ভাবনা ছিল। কিন্তু প্রথম কয়েক বছর নাৎসিরা কোনো উৎপাত করলো না। ১৯৪৩ সালে নাৎসিরা ডেনমার্কের ইহুদীদের কনসেন্ট্রেশন ক্যাম্পে নিয়ে যেতে শুরু করলো। প্রাণভয়ে নৌপথে স্বপরিবারে সুইডেন চলে এলেন বোর। এক সপ্তাহ পরেই তারা যুক্তরাজ্যে চলে যান এবং দ্বিতীয় বিশ্বযুদ্ধ শেষ হওয়া পর্যন্ত সেখানেই বসবাস করেন।
নীলস বোরের জন্ম ১৮৮৫ সালের ৭ অক্টোবর, ডেনমার্কের রাজধানী কোপেনহেগেনে। তার বাবা ক্রিশ্চিয়ান বোর ছিলেন একজন বিখ্যাত ফিজিওলজি অধ্যাপক, যিনি দু’বার নোবেল পুরস্কারের জন্য মনোনীত হয়েছিলেন। তার মা এডলারও ছিলেন উচ্চশিক্ষিতা। ৭ বছর বয়সে বোরকে গ্রামার স্কুলে ভর্তি করানোর আগেই তার বাবা-মা অনুধাবন করতে পেরেছিলেন বোরের মেধা কত প্রখর। তাই ছেলেকে বিজ্ঞানী করবেন বলেই ঠিক করেন তারা। পাশাপাশি একজন রুচিসম্পন্ন মানুষ হিসেবে গড়ে তুলতে, সমৃদ্ধ সাহিত্য শিক্ষারও ব্যবস্থা করা হয় বোরের জন্য।

নীলস বোর (১৮৮৫-১৯৬২); source: feelgrafix.com
কোপেনহেগেন বিশ্ববিদ্যালয়ে বোর জ্যোতির্বিদ্যা, পদার্থবিদ্যা, রসায়ন এবং গণিত নিয়ে পড়েন। ১৯০৭ সালে তিনি সেখান থেকে বি. এস ডিগ্রি সম্পন্ন করেন। ১৯০৭-১১ সালে তিনি পদার্থবিজ্ঞানে এম.এস এবং পি.এইচডি করেন। নিজের জীবনের শ্রেষ্ঠ আবিষ্কারের বছর, অর্থাৎ ১৯১২ সালে বোর, মার্গারেথ নোরলান্ডকে বিয়ে করেন। এই সুখী দম্পতির ঘরে ৬ সন্তানের জন্ম হয়েছিল। এই ছয়জনের একজন, অ্যাইজ বোরও পিতার মুখ উজ্জ্বল করে পদার্থবিজ্ঞানে জিতেছিলেন নোবেল পুরস্কার।
১৯৬২ সালের ১৮ নভেম্বর এই মহান বিজ্ঞানী মৃত্যুবরণ করেন। কোপেনহেগেনের অ্যাসিস্টেনস সমাধিক্ষেত্রে তাকে সমাহিত করা হয়।
ফিচার ছবি: feelgrafix.com








